
Подробный официальный разбор заданий Всероссийской олимпиады школьников по Химии от 22-23 января 2026 г. Решения, критерии оценивания и комментарии экспертов для 10 класса.
Задания для 10 класса
Скачать задания первого тура для 10 класса
Скачать задания практического тура для 10 класса
Критерии для 10 класс
Скачать критерии первый тур для 10 класса
Скачать критерии практического тура для 10 класса
Репетиторский центр «Беззубрежкин» г. Калуга
Региональный этап по Химии 10 класс
Задание 1. Токсичная задача
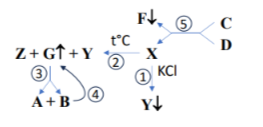
Токсичная белая соль X ограниченно растворима в воде. При добавлении к ее насыщенному раствору концентрированного раствора хлорида калия выпадает осадок токсичной соли Y (р-ция 1).
Соль X разлагается при 150 °C с образованием трех продуктов: соли Y, токсичного твердого бинарного соединения Z и токсичного жёлто-зеленого газа G (р-ция 2). Масса соли Y, которая образуется при разложении X, в 7 раз меньше, чем получается при осаждении раствором хлорида калия из такого же количества Х.
При растворении в воде жёлто-зеленый газ G очень медленно реагирует с ней, образуя смесь двух токсичных кислот A и B (р-ция 3). Кислота В неустойчива и разлагается с выделением газа G (р-ция 4).
Соль X была получена путем взаимодействия в разбавленном водном растворе двух токсичных солей C и D. При этом в осадок выпала белая нетоксичная и нерастворимая в кислотах соль F (р-ция 5). Соль D используется в пиротехнике и придает фейерверку зеленую окраску. Из 3.04 г соли D образуется 5.75 г соли Х.
Вопросы:
Предложите ещё один способ получения газа G? Запишите уравнение реакции.
Определите формулу газа G. Получите с помощью расчета формулы веществ X, Y, Z
Запишите уравнения реакций 1 – 5.
Задание 2. С открытием радиоактивности появилось много различных изотопов элементов, которые тогда считали самостоятельными элементами. Таблица Д.И. Менделеева не могла их всех вместить и даже названий не хватало, поэтому их стали называть по элементу, в продуктах распада которого они обнаруживались. Так появились Радий В (RaB), Радий A (RaA), Торий D (ThD), Мезаторий-1 (MsTh1) и многие другие. В природе элемент Q представлен в основном изотопом RaF (T1/2 = 138 дней), который при альфа-распаде превращается в стабильный RaG. Радий входит в ряд радиоактивного распада, который начинается с 238U (T1/2 = 4.468·109 лет1).
Простое вещество, состоящее из изотопа RaF, реагирует с хлором при нагревании, при этом образуется смесь соединений X и Y (р-ции 1 и 2). Соединения X и Y – твердые вещества красно-рубинового и лимонно-желтого цвета, соответственно. При нагревании в вакууме Y превращается в X, а потеря массы при этом составляет 20.15 % (р-ция 3).
При добавлении к водному солянокислому раствору Y раствора хлорида аммония выпадает осадок комплексной соли Z (р-ция 4). При пропускании сероводорода через раствор Y выпадает осадок A, содержащий RaF (р-ция 5), который растворяется в концентрированной соляной кислоте (р-ция 6). Осадок А аналогично может быть выделен и из раствора Х.
Взаимодействие Y (А = 3.70·1010) с избытком 0.5 М раствора азотной кислоты приводит к образованию белого кристаллического осадка B массой 346±1 мкг2 (р-ция 7).
После отделения осадка и высушивания вакууме при комнатной температуре полученное вещество проанализировали на содержание нитрат-ионов. В пробе обнаружили 1.59 мкмоль нитрат-ионов. В реакции Y с азотной кислотой с.о. RaF не изменяется.
Дополнительная информация:
Активность A = λ N, [Бк] =[распад/с], где 𝜆 = 0.69315/𝑇1/2 – вероятность распада ядра в единицу времени, с-1, N – количество атомов радиоактивного изотопа. Удельная активность Ауд = A/𝑚
соли Z равна 7.628·1013 Бк/г. RaG образует соль, имеющую такие же состав и строение, что и соль Z.
За долгое время устанавливается так называемое «вековое равновесие», при котором активности (А) всех радиоактивных изотопов образующихся из 238U равны.
Вопросы:
Какое количество вещества RaF (моль) содержится в 1 тонне урановой руды, если массовая доля урана в ней составляет 0.205%, а массовая доля изотопа 238U в природной смеси составляет 99.3%.
Расшифруйте RaF и RaG, если известно, что в природных радиоактивных рядах только α и β — распады приводят к изменению порядкового номера и массы элемента.
Запишите уравнения описанных реакций и приведите формулы веществ X, Y, Z, A и B.
Задание 3. “Ultra” (за) + “Marinus” (морской) = “Y” (заморский)
Простое вещество X растворяется в бензоле, сероуглероде, взаимодействует с концентрированным раствором гидроксида металла M с образованием A (р-ция 1).
Ярко-желтое вещество В можно получить тремя способами: (I) Нагреванием твердых А и X в запаянной ампуле при 500°С до образования гомогенного расплава с последующим медленным охлаждением и кристаллиза- цией (р-ция 2); (II) Кипячением с обратным холодильником спиртового раствора C и стехиометрического количества металла M в инертной атмосфере (р-ция 3); (III) Нагреванием твёрдых A и C при 200°С, взятых в соотношении 8 : 9 по массе, соответственно (р-ция 4).
Желтые кристаллы В реагируют с порошком X в мольном соотношении 4 к 1, соответственно, с образованием оранжевых кристаллов вещества С.
Галогениды щелочных металлов могут быть использованы для стабилизации анион-радикалов D и E.
Так, бесцветные кристаллы иодида калия способны менять окраску в присутствии паров X на желтую при внедрении D (р-ция 5) или синюю при внедрении E (р-ция 6).
С древних времен известен интенсивно-синий пигмент Y. Его окраска обусловлена наличием анион- радикалов D и E, которые замещают хлорид-анионы, в структуре минерала Z.
Вопросы и задания:
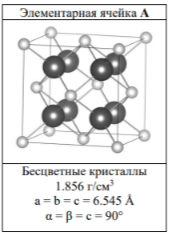
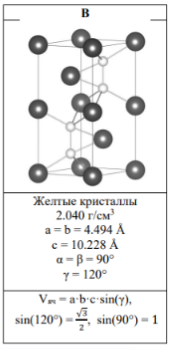
Определите состав X, неизвестные вещества A – С, состав 33e—частицы D и 49e—частицы E. Ответ обоснуйте.
Запишите уравнения реакций 1-6. Реакции 5-6 запишите в сокращенной ионной форме.
Определите формулу алюмосиликата Z с минимальными целыми индексами, если массовые доли Na, Al, Si и Cl равны 18.98%, 16.70%, 17.39% и 7.31%, соответственно.
Укажите название пигмента Y. Какого цвета будет Z при эквимолярном соотношении внедрений D и E в его структуре?
Задание 3. Уроборос
Уробóрос – свернувшийся в кольцо змей или дракон, кусающий себя за хвост. Является одним из древнейших символов, известных человечеству.
В растворе ω-гидроксиальдегиды HO–(CH2)n–CHO существуют в виде смеси двух таутомеров: циклического (C) и линейного (L); содержание енольной формы в большинстве растворителей пренебрежимо мало. Соотношение между линейной и циклической формами зависит от температуры, растворителя и величины n.
В таблице приведены экспериментально определённые мольные доли линейной формы в водно-диоксановых растворах ω-гидроксиальдегидов с n = 3, 4 и 5:
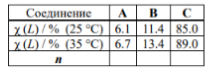
Сопоставьте соединения A–C со значениями n. Ответ объясните.
Вычислите значения констант равновесия для процесса превращения L в C при 25 °C для всех трёх соединений.
Определите знаки величин ΔrH° и ΔrS° для процесса превращения L в C. Ответ объясните.
Вычислите эти величины для вещества С. Какой фактор – энтальпийный или энтропийный контролирует образование циклической формы? Ответ объясните.
С учётом ошибки эксперимента измеренная χ (L) для C составляет 85.0 ± 1.0 % при 25 °C и 89.0 ± 1.0 % при 35 °C. Принимая во внимание эти ошибки, оцените, насколько величины K, ΔrH° и ΔrS° могут отклоняться от средних значений, полученных в вопросах 2 и 3, если температура измерена точно. Как можно повысить точность определения ΔrH° и ΔrS°, если точность определения констант равновесия невозможно повысить?
В действительности в растворе в равновесии находятся не две, а три изомерные формы гидроксиальдегида (если пренебречь содержанием енольной формы). Объясните этот факт и рассчитайте константы равновесия взаимопревращений трёх форм для соединения B при 25 °C.