
Подробный официальный разбор заданий Всероссийской олимпиады школьников по Химии от 22-23 января 2026 г. Решения, критерии оценивания и комментарии экспертов для 11 класса.
Задания для 11 класса
Скачать задания первого тура для 11 класса
Скачать задания практического тура для 11 класса
Критерии для 11 класс
Скачать критерии первый тур для 11 класса
Скачать критерии практического тура для 11 класса
Репетиторский центр «Беззубрежкин» г. Калуга
Региональный этап по Химии 11 класс
Задание 1. «Серебряный век» химических равновесий
Химик Колбочкин нашёл в архивах старые записи ученого, пытавшегося охарактеризовать химические равновесия в водной суспензии оксида серебра(I).
К сожалению, часть записей стерлась от времени. Помогите Колбочкину восстановить пропуски в записях и ответьте на поставленные вопросы.
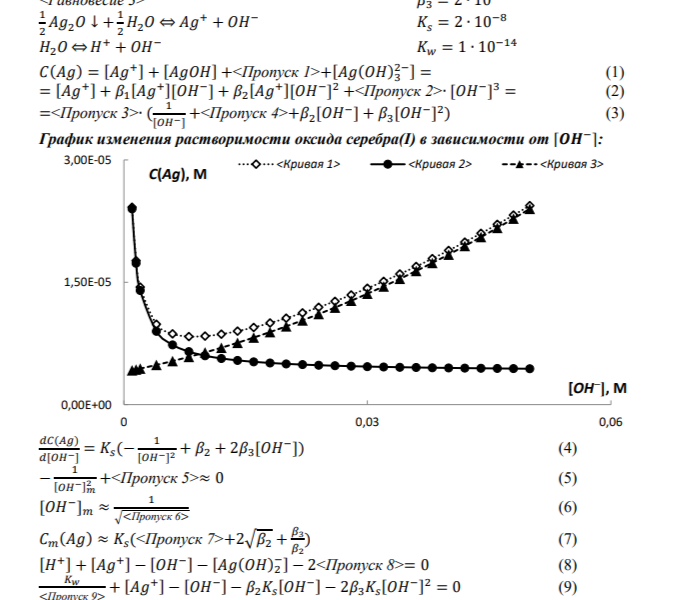
Вопросы:
Что должно быть вместо Пропусков 1–10 в записях ученого? Запишите ответы.
Какими химическими уравнениями описываются Равновесия 1–3? Запишите их.
Какая из Кривых 1–3 отвечает растворимости оксида серебра(I)?
Какими математическими выражениями описываются две другие кривые? Запишите эти выражения.
Какое значение pH создается в водной суспензии оксида серебра(I)?
Вычислите при каком значении рН = –lg[H+] = 14 – lg[OH–] в диапазоне 0 – 14 растворимость оксида серебра(I) будет минимальна?
Рассчитайте минимальную концентрацию (в моль/л) растворенного серебра над осадком его оксида, которой можно достичь, варьируя рН в диапазоне 0 – 14?
В 1 литре воды приготовили суспензию 𝐴𝑔2𝑂, рассчитайте сколько грамм осадка растворится?
Сколько грамм NaOH нужно добавить к суспензии оксида серебра в воде, чтобы масса осадка осталась неизменной? Ответ не равен нулю.
Задание 2. Около 100 лет назад был открыт один из самых редких и рассеянных элементов Х.
В природной смеси изотопов natX содержатся: стабильный 𝐴𝑍𝐗 (37.40 %, с четным числом нейтронов) и радиоактивный 𝐴+𝑍2𝐗 (62.60 %, Т1/2 = 43.5 млрд лет), продуктом распада которого является стабильный нуклид Q* одного из благородных металлов.
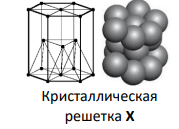
Плотность Х 21.03 г/см3, радиус атома 1.375 Å. Металл Х кристаллизуется в плотнейшей гексагональной упаковке (см. рисунок расстояния между всеми соседним атомами одинаковые).
Максимальные количества элемента Х (до 0.1 %) обнаружены в молибдените (𝜔Мо = 59.94%) (можно рассматривать как смесь молибденита с изоморфным ему Х1), который является основным источником X. При обжиге молибденита в том числе образуется летучее соединение X2, (р-ции 1, 2), которое концентрируется в продуктах пылеуловительных систем в виде светло-желтого кристаллического вещества, которое взаимодействует с горячей водой с образованием сильной кислоты X3 (р-ция 3). Плохо растворимая аммонийная соль этой кислоты при нагревании восстанавливается водородом с образованием металла X (р-ция 4).
При взаимодействии калиевой соли кислоты Х3 (m = 1.100 г) со смесью концентрированных бромоводородной и фосфорноватистой кислот с последующим добавлением бромида цезия выпадают черные пластинчатые кристаллы (m = 2.210 г, выход 91%) комплексной соли X4 (р-ция 5 – последовательные стадии запишите одним уравнением). Анион соли Х4 является биядерным кластером без мостиковых атомов с двумя удивительными особенностями: очень коротким расстоянием X – X (2.24 Å) и заслоненной конфигурацией лигандов.
Пара нуклидов 𝐴+𝑍2𝐗 /Q* нашла применение в геохронологии, так как в молибденитах элемент Q отсутствует, а накапливается исключительно радиогенный Q. Поэтому по соотношению атомов элементов Х и Q можно рассчитать возраст минерала.
Так в карельских молибденитах соотношение атомов natX и Q составляет 35 : 1.
Вопросы.
Определите возраст карельского молибденита.
Рассчитайте объём элементарной ячейки металла Х. (выведите все необходимые формулы! Ответ без вывода формул не оценивается)
Определите металл Х, его природные нуклиды, формулу молибденита и соединений Х1 – Х4. Ответ подтвердите расчетами.
Запишите уравнения реакций 1 – 5. Запишите упомянутое в задаче уравнение радиоактивного распада 𝐴+𝑍2𝐗 с образованием Q.
Задание 3. Растворимость CO2 в воде и в море
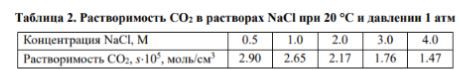
Растворение углекислого газа в воде играет важную роль не только в пищевой промышленности, но и в формировании всей экосистемы Земли. Изучим этот процесс с точки зрения термодинамики и кинетики. В табл. 1 приведены экспериментальные данные.

Назовите ещё один газ, кроме CO2, растворимость которого в воде определяет состояние биосферы. Сравните растворимость этого газа с растворимостью CO2 и объясните различие.
При какой из указанных в таблице температур растворимость газа ближе всего к значению 1 объём CO2 : 1 объём воды? Ответ подтвердите расчётом.
Приведите выражение для константы равновесия CO2(г) ⇄ CO2(р-р) и найдите её значение при 25 °C. В качестве стандартных примите давление 1 атм и концентрацию 1 моль/л.
Используя данные таблицы 1, рассчитайте энтальпию растворения CO2 в воде. Примите, что она не зависит от температуры. Для расчёта можно выбрать любые две температуры.
Найдите pH насыщенного раствора CO2 в воде при 25 °C. Константы диссоциации H2CO3: K1 = 4.5⋅10–7, K2 = 4.70⋅10–11.
Для изучения кинетики растворения CO2 в воде термостатируемый металлический цилиндр при 25 °C заполнили наполовину дистиллированной водой, а в оставшуюся половину быстро ввели углекислый газ до давления 1 атм. После этого измеряли зависимость давления над раствором от времени. Оказалось, что растворение газа отлично описывается кинетикой 1-го порядка.
Постройте качественно график зависимости pH раствора от времени, от начала опыта до установления равновесия. На оси ординат укажите не менее двух числовых значений.
Таблица 2 характеризует зависимость растворимости CO2 в солевых растворах от концентрации соли. Даны три водоёма: озеро Байкал, Чёрное море и Красное море.
Расположите эти водоёмы в ряд по увеличению концентрации CO2 в них в июле месяце.
Объясните ответ.
Задание 4. И снова четыре элемента…
Молекулярные формулы четырёх веществ XA–XD, содержат атом одного из расположенных в одной группе Периодической системы элементов A–D, соответственно, и один и тот же общий фрагмент. Молекулярные массы этих соединений относятся как 1 : 1.236 : 1.925 : 2.64, соответственно. Для синтеза соединений XA–XD используются два основных вида сырья. Эти виды сырья могут быть описаны с помощью ассоциативных рядов 1 и 2, расположенных в приложении к задаче.
При кипячении сырья 1 с концентрированной серной кислотой образуется соединение EA, которое при повышенной температуре разлагается с образованием равных количеств XA и монооксида углерода. Вещество XB получают обработкой XA неприятно пахнущим газом F при 400 °C в присутствии оксида алюминия. При сгорании F в недостатке кислорода на стенках сосуда образуется жёлтый налёт простого вещества.
Основной компонент сырья 2 – вещество G – при температуре 1500 °С разлагается с образованием бесцветного газа H, из которого в четыре стадии можно получить соединение XD. На первом шаге H обрабатывают избытком формальдегида в присутствии карбида меди. Продуктом этой реакции является соединение I, при взаимодействии которого с хлористым тионилом в хлористом метилене при –30 °С в присутствии пиридина образуется вещество J. Его обработка избытком горячего этанольного раствора гидроксида калия позволяет получить вещество K, имеющее такой же качественный состав, что и H, но практически в два раза большую молекулярную массу. Взаимодействие K с натриевой солью элемента D в метаноле позволяет получить соединение XD. В то же время единственным продуктом взаимодействия некоторого красного простого вещества и газа H при 400 °C является соединение XC.
Химические свойства соединений XA–XD во многом схожи, хотя есть и различия.
Например, при взаимодействии с N,N-диметилформамидом в присутствии оксихлорида фосфора с последующим гидролизом все они дают соответствующие продукты EA–ED однотипного строения, отличающиеся только атомами элементов A–D. При взаимодействии с ацетилнитратом XB и XC образуют однотипные продукты LB и LC, соответственно. В то же время XD с ацетилнитратом не реагирует, а XA даёт продукт M, который можно затем превратить в LA при действии пиридина. XA реагирует с малеиновым ангидридом при комнатной температуре с образованием продукта NA. В случае XB аналогичный продукт NB образуется только в жёстких условиях (100 °C, 15 кбар). При взаимодействии XC с малеиновым ангидридом в жёстких условиях получается продукт O, который вообще не содержит элемента C, а XD с малеиновым ангидридом не реагирует.
Вопросы:
Какие два вида сырья используются для синтеза веществ XA–XD в задаче? Не забудьте подтвердить ваш ответ логическими рассуждениями.
Установите состав соединений XА–XD, F–K, M и O. Если вещество обладает изомерией, приведённая вами формула должна однозначно отражать порядок связи атомов в молекуле. Для трёх наборов веществ EA–ED, LA–LC и NA–NB приведите структурные формулы для одного любого вещества из каждого набора (например, можно привести структуры соединений EA, LA и NA).
Дополнительная информация: а) региоселективность образования продуктов EA–ED и LB–LC определяется устойчивостью катионных интермедиатов этих реакций; б) вещество M содержит 41.6 масс. % углерода и не имеет в своей структуре связей C=C, сопряжённых с другими кратными связями или неподелёнными парами гетероатомов; в) соединение O образуется в результате распада NC.
Укажите тривиальные названия веществ XA–XD.
Поясните, с чем связана различная реакционная способность соединений XA–XD по отношению к малеиновому ангидриду.

