
На официальном сайте Всероссийской олимпиады школьников представлены задания и ответы школьного этапа олимпиады по Химии для учеников 9 классов, группа 3, запланированный на 6 октября 2022 года. Получите доступ к полной информации о заданиях, проверьте свои знания и подготовьтесь к успешному выступлению на олимпиаде. Участвуйте и достигайте новых успехов в области информатики!
?Список заданий «Сириус» по Химии 9 класс — 3 группа?
1. Определите, какие водные растворы изображены на рисунках.
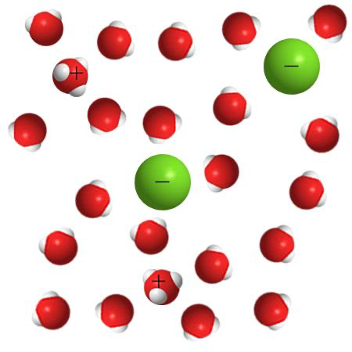
Раствор щёлочи
Раствор сильной кислоты
Раствор слабой кислоты
Раствор соли
Раствор неэлектролита
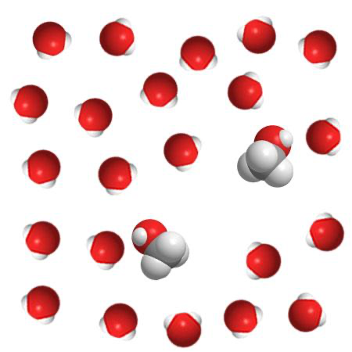
Раствор щёлочи
Раствор сильной кислоты
Раствор слабой кислоты
Раствор соли
Раствор неэлектролита
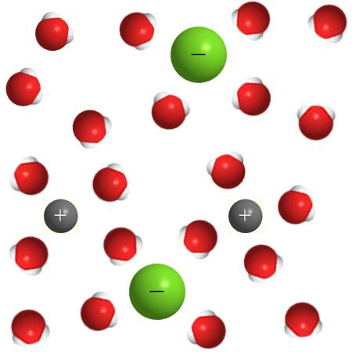
Раствор щёлочи
Раствор сильной кислоты
Раствор слабой кислоты
Раствор соли
Раствор неэлектролита
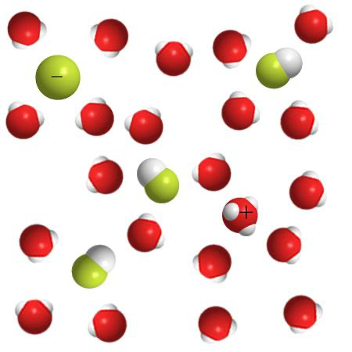
Раствор щёлочи
Раствор сильной кислоты
Раствор слабой кислоты
Раствор соли
Раствор неэлектролита
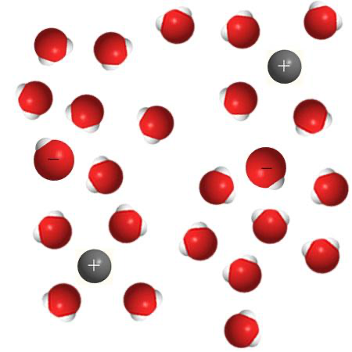
Раствор щёлочи
Раствор сильной кислоты
Раствор слабой кислоты
Раствор соли
Раствор неэлектролита
2. В воде растворили 0.2 моль вещества. В полученном растворе общее количество положительных и отрицательных ионов превышает 0.55 моль. Какое вещество могло быть растворено? Выберите все верные ответы:
Ca(NO3)2
HCl
BaSO4
Cu(OH)2
Na2SO4
FeSO4
3. Решите химический кроссворд. Ответами являются химические формулы веществ. Каждую букву и цифру формулы вещества необходимо записать в отдельную строку справа.
Ядовитый газ, образующийся при неполном сгорании топлива.
Пищевая сода.
Самый лёгкий газ среди сложных веществ.
Ион, образующися при диссоциации азотной кислоты.
Трёхосновная кислота.
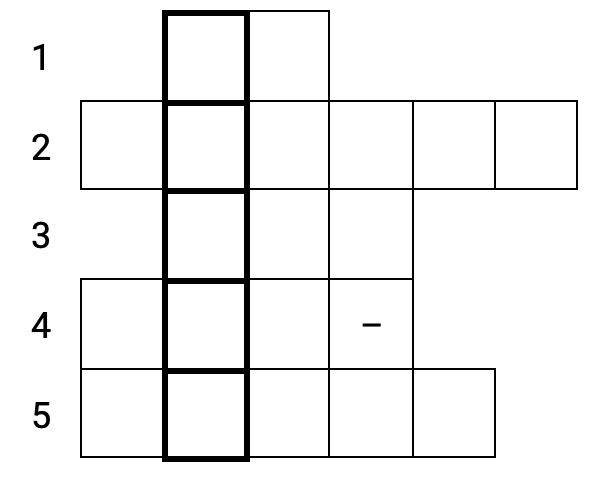
В выделенной области у вас должна получиться формула широко используемого в искусстве и в строительстве минерала. Запишите название минерала, состоящее из 6 букв, в именительном падеже:
4.Установите соответствие между описанием реакции и реагирующими веществами.
При смешении двух бесцветных растворов выпадает жёлтый осадок
В водном растворе не протекает
Является окислительно-восстановительной
KI и Pb(NO3)2
FeCl2 и Na2S
KI и AgNO3
FeCl3 и H2S
HCl и AgNO3
NaNO3 и BaCl2
5. Смеси гелия с кислородом под общим названием «Гелиокс» используют для глубоководных погружений и лечения заболеваний дыхательных путей. Гелиокс 60/40 содержит 60 % гелия по объёму. Во сколько раз он тяжелее чистого гелия (при одинаковых условиях)? Ответ округлите до десятых.
6. Неизвестное вещество X состоит из ионов, имеющих такую же электронную конфигурацию, как и атом неона. Оно представляет собой белый порошок, реагирующий с соляной кислотой с образованием бесцветного раствора. При действии на полученный раствор гидроксидом натрия выпадает белый осадок, нерастворимый в избытке щёлочи.

Сколько всего электронов находится на p‑орбиталях в атоме неона?
Запишите химическую формулу вещества X.
При спекании вещества X с оксидом алюминия образуется бесцветное вещество, встречающееся в природе в виде минерала Y. Запишите формулу этого минерала, если известно, что X реагирует с оксидом алюминия в мольном соотношении 1:1.
7. В ёмкости находится бесцветный раствор. При выливании на керамическую плитку спустя некоторое время он самопроизвольно загорается. Горение сопровождается выделением белого дыма и образованием синего пламени. Твёрдого нелетучего остатка от сгорания не остается. Продукты сгорания при пропускании их над безводным сульфатом меди (II) не вызывают изменения его окраски.
Выберите возможный растворитель:
Этиловый спирт C2H5OH
Вода
Сероуглерод CS2
Гексан C6H14
Выберите возможное растворённое вещество:
Cера S
Белый фосфор P4
Хлорид натрия NaCl
Метан CH4
Белый дым при остывании оседает в виде белого порошка. Найдите массу этого порошка, образующегося при сгорании 124 г 10 %‑го исследуемого раствора. Ответ выразите в граммах, округлите до десятых.
8.В пробирках выданы растворы следующих солей натрия: хлорид, карбонат, силикат, сульфид и фосфат. Из каждой пробирки отобрали пробы растворов объёмом 1 мл, к которым добавили соляную кислоту. В таблице представлены результаты эксперимента:
Выделился газ без цвета и без запаха
Карбонат натрия
Фосфат натрия
Хлорид натрия
Силикат натрия
Сульфид натрия
Выпал бесцветный студнеобразный осадокКарбонат натрия
Фосфат натрия
Хлорид натрия
Силикат натрия
Сульфид натрия
Выделился бесцветный газ с неприятным запахомКарбонат натрия
Фосфат натрия
Хлорид натрия
Силикат натрия
Сульфид натрия
Без изменений; после добавления раствора CaCl2 также без измененийКарбонат натрия
Фосфат натрия
Хлорид натрия
Силикат натрия
Сульфид натрия
Без изменений; после добавления раствора CaCl2 выпал белый осадокКарбонат натрия
Фосфат натрия
Хлорид натрия
Силикат натрия
Сульфид натрия
Каждому опыту поставьте в соответствие исследуемое вещество.
9. Для разрыва химической связи в молекулах H2 и Cl2 требуется 218 и 120 единиц энергии соответственно, а при образовании одной молекулы HCl из атомов H и Cl выделяется 215 единиц энергии. Сколько единиц энергии выделяется при образовании 2 молекул HCl из молекул H2 и Cl2? Ответ округлите до целых.
10. На химическом производстве используют смесь двух газов, плотность которой в 2 раза меньше плотности смеси равных объёмов азота и кислорода (при одинаковых условиях). При сгорании этой смеси образуются газ, вызывающий помутнение известковой воды, и бесцветная жидкость, которая при добавлении к безводному сульфату меди (II) придаёт веществу синюю окраску.
Запишите в любом порядке формулы газов, входящих в состав искомой смеси.
Сколько молекул более тяжелого газа приходится на одну молекулу более лёгкого газа в смеси?
Число
Чему равна относительная плотность смеси по водороду? Ответ округлите до десятых.
11. В лаборатории провели три опыта.Опыт 1. В пробирку (см. рисунок) поместили вещество А жёлто‑оранжевого цвета и нагрели. Из пробирки выделялся газ Б, не имеющий ни цвета, ни запаха, поддерживающий горение. В пробирке остались капельки металла В серебристого цвета. Металл В не реагирует ни с соляной кислотой, ни с разбавленной серной кислотой.
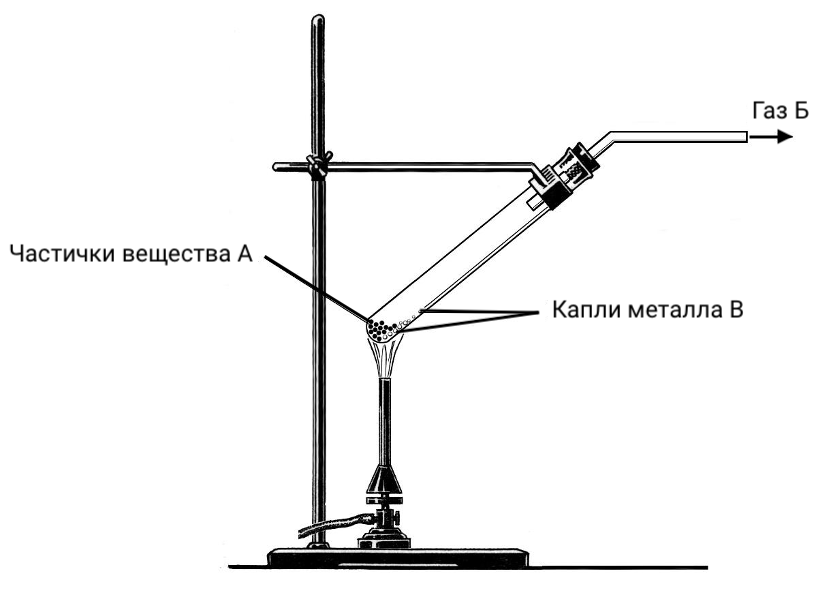
Опыт 2. Вещество А растворили в соляной кислоте и получили бесцветный раствор вещества Г. Часть раствора Г перенесли в пробирку и пропустили через него сероводород, при этом наблюдали выпадение в осадок вещества Д чёрного цвета. Вещество Д встречается в природе. Кристаллы природного Д могут иметь красную окраску.
Опыт 3. Во вторую часть раствора Г внесли хорошо зачищенную медную пластинку. На поверхности пластинки выделился блестящий слой металла В.
Известно, что Б и В — простые вещества. Вещества А, Г и Д состоят из двух элементов. Вещества А, Г и Д содержат атомы одного и того же химического элемента со степенью окисления +2.
Определите вещества А–Д и запишите их формулы.
**А**
**Б**
**В**
**Г**
**Д**
12. Круглодонную колбу объёмом 1.000 л закрыли пробкой с газоотводной трубкой и заполнили газом X при н.у. Масса газа в колбе составила 5.714 г. Затем газоотводную трубку опустили в кристаллизатор с водой (на рисунке показан цифрой 1), в которую был добавлен фиолетовый лакмус. Открыли кран (2), и вода по трубке стала подниматься вверх, внутри колбы «забил фонтан».
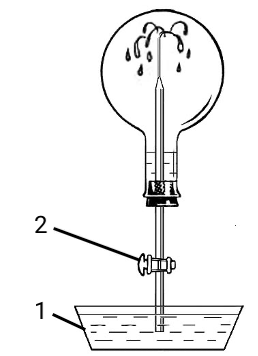
Лакмус в растворе внутри колбы принял красную окраску. Для того, чтобы лакмус снова принял фиолетовую окраску, потребовалось добавить в раствор 2.500 г гидроксида калия.
Определите газ X и запишите его формулу.
норм