
Официальный образец варианта заданий с ответами и решениями ВПР 2025 по Химии 8 класс с официального ресурса ФИОКО (Федеральный институт оценки качества образования). Демоверсия предназначена для подготовки учащихся к всероссийской проверочной работе (ВПР), которая пройдет в период с 11 апреля по 16 мая 2025 года.
→ Типовые (тренировочные варианты) по Химии 8 класс
→ Образец проверочной работы по Химии 8 класс
→ Описание проверочной работы по Химии 8 класс
Онлайн вариант ВПР 2025 по Химии 8 класс
Назначение всероссийской проверочной работы
Всероссийские проверочные работы (ВПР) проводятся в целях осуществления мониторинга уровня и качества подготовки обучающихся в соответствии с требованиями федеральных государственных образовательных стандартов и федеральных основных общеобразовательных программ. Назначение ВПР по учебному предмету «Химия» – оценить качество общеобразовательной подготовки обучающихся 8 классов в соответствии с требованиями федерального государственного образовательного стандарта основного общего образования (ФГОС ООО) и федеральной образовательной программы основного общего образования (ФОП ООО).
Структура проверочной работы
Проверочная работа состоит из двух частей и включает в себя 9 заданий. В части 1 содержатся задания 1–5; в части 2 – задания 6–9. Задания проверяют сформированность системы знаний о химических веществах и их превращениях, а также умений применять химические знания при решении практических задач. Задания 1, 2, 7.3 основаны на изображениях конкретных объектов и/или процессов и требуют анализа этих изображений. Задание 5 построено на основе справочной информации и предполагает анализ реальной жизненной ситуации. Задания 1, 3.1, 4, 6.2, 6.3, 8 и 9 требуют краткого ответа. Остальные задания проверочной работы предполагают развернутый ответ.
Инструкция по выполнению работы
На выполнение заданий части 1 проверочной работы по химии отводится один урок (не более 45 минут). Часть 1 включает в себя 5 заданий. При выполнении работы разрешается использовать следующие дополнительные материалы: – Периодическая система химических элементов Д.И. Менделеева; – таблица растворимости кислот, солей и оснований в воде; – ряд активности металлов / электрохимический ряд напряжений металлов; – непрограммируемый калькулятор. Ответы на задания запишите в поля ответов в тексте работы. В случае записи неверного ответа зачеркните его и запишите рядом новый. При необходимости можно пользоваться черновиком. Записи в черновике проверяться и оцениваться не будут. Советуем выполнять задания в том порядке, в котором они даны. В целях экономии времени пропускайте задание, которое не удаётся выполнить сразу, и переходите к следующему. Если после выполнения всей работы у Вас останется время, то Вы сможете вернуться к пропущенным заданиям.
Задания проверочной работы по Химии
Задание 1.1. Внимательно рассмотрите предложенные рисунки. Укажите номер рисунка, на котором изображён объект, содержащий индивидуальное химическое вещество.

Задание 1.2. Какие вещества содержатся в объектах, изображённых на остальных рисунках? Приведите по ОДНОМУ примеру. Для каждого вещества укажите его химическое название и формулу.
Задание 2. Превращение одних веществ в другие называется химической реакцией.
Задание 2.1. Из представленных ниже рисунков выберите тот, на котором изображено протекание химической реакции.
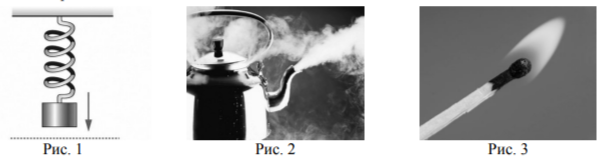
Протекание химической реакции изображено на рисунке:
Задание 2.2. Укажите один ЛЮБОЙ признак протекания этой химической реакции:
Задание 2. Превращение одних веществ в другие называется химической реакцией.
Задание 2.1. Укажите, какой из приведённых ниже процессов является химической реакцией.
1) распространение аромата цветов в комнате
2) движение маятника в механических часах
3) образование накипи в чайнике при кипячении водопроводной воды
Задание 2.2. Укажите один ЛЮБОЙ признак протекания этой химической реакции:
Задание 3. В таблице приведены названия и химические формулы некоторых газообразных веществ.
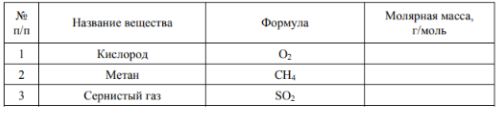
Задание 3.1. Используя предложенные Вам справочные материалы, вычислите молярные массы каждого из газов и запишите полученные данные в таблицу.
Задание 3.2. Каким из приведённых в таблице газов следует наполнить шарик с практически невесомой оболочкой, чтобы он оказался легче воздуха и смог взлететь? (Средняя молярная масса воздуха равна 29 г/моль.). Укажите номер вещества.
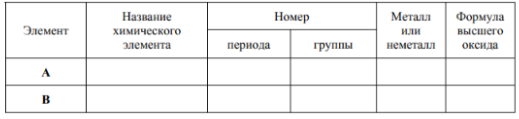
Задание 4. Даны два химических элемента: А и В. Известно, что в атоме элемента А содержится 12 протонов, а в атоме элемента В – 16 электронов.
Задание 4.1. Используя Периодическую систему химических элементов Д.И. Менделеева, определите химические элементы А и В.
Задание 4.2. Укажите номер периода и номер группы в Периодической системе химических элементов Д.И. Менделеева, в которых расположен каждый элемент.
Задание 4.3. Установите, металлом или неметаллом являются простые вещества, образованные этими химическими элементами.
Задание 4.4. Составьте формулы высших оксидов, которые образуют элементы А и В.
Задание 5. Восьмиклассник Никита выпил после обеда один стакан (200 г) яблочного сока.
Задание 5.1. Используя данные приведённой ниже таблицы, определите, какую массу углеводов получил при этом организм юноши. Ответ подтвердите расчётом.
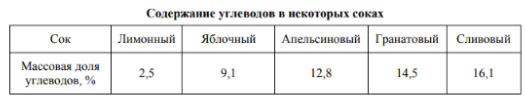
Задание 5.2. Какую долю суточной физиологической нормы углеводов (360 г) получил Никита, выпив стакан яблочного сока? Ответ подтвердите расчётом.
Инструкция по выполнению заданий части 2 проверочной работы
На выполнение заданий части 2 проверочной работы по химии отводится один урок (не более 45 минут). Часть 2 включает в себя 4 задания. При выполнении работы разрешается использовать следующие дополнительные материалы: – Периодическая система химических элементов Д.И. Менделеева; – таблица растворимости кислот, солей и оснований в воде; – ряд активности металлов / электрохимический ряд напряжений металлов; – непрограммируемый калькулятор. Ответы на задания запишите в поля ответов в тексте работы. В случае записи неверного ответа зачеркните его и запишите рядом новый. При необходимости можно пользоваться черновиком. Записи в черновике проверяться и оцениваться не будут. Советуем выполнять задания в том порядке, в котором они даны. В целях экономии времени пропускайте задание, которое не удаётся выполнить сразу, и переходите к следующему. Если после выполнения всей работы у Вас останется время, то Вы сможете вернуться к пропущенным заданиям.
Задание 6. Имеется следующий перечень химических веществ: калий, хлор, алюминий, водород, хлорид калия, серная кислота, сульфат алюминия. Используя этот перечень, выполните задания 6.1–6.5.
Задание 6.1. Напишите химические формулы каждого из указанных веществ: Калий – Хлор – _ Хлорид калия – _ Алюминий – _ Серная кислота – _ Сульфат алюминия – _ Водород – _
Задание 6.2. Какое из веществ, упоминаемых в перечне, соответствует следующему описанию: «Ядовитый газ жёлто-зелёного цвета, тяжелее воздуха, с резким запахом»?
Задание 6.3. Из данного перечня выберите ЛЮБОЕ СЛОЖНОЕ вещество. Запишите его химическую формулу и укажите, к какому классу неорганических соединений оно относится:
Задание 6.4. Из приведённого перечня веществ выберите ЛЮБОЕ соединение, состоящее из атомов ТРЁХ элементов. Вычислите массовую долю кислорода в этом соединении.
Задание 6.5. Вычислите массу 0,5 моль газообразного водорода.
Задание 6.5. Вычислите, сколько молекул содержится в 0,5 моль газообразного водорода.
Задание 7. Ниже даны словесные описания двух химических превращений с участием веществ, перечень которых был приведён в задании 6: (1) калий + хлор → хлорид калия; (2) алюминий + серная кислота (разб.) → сульфат алюминия + водород.
Задание 7.1.Составьте уравнения указанных реакций, используя химические формулы веществ из п. 6.1:
Задание 7.2. В зависимости от количества и состава веществ, вступающих в химическую реакцию и образующихся в результате неё, различают реакции соединения, разложения, замещения и обмена. Выберите ЛЮБУЮ из реакций (1) или (2) и укажите её тип.
Задание 7.3. Из приборов, изображённых на рисунках, выберите тот, с помощью которого можно получить и собрать газообразный водород по реакции (2).
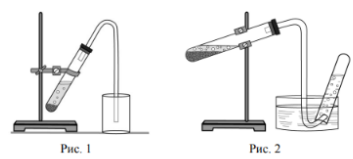
Водород можно получить и собрать с помощью прибора, изображённого на рисунке:
Каким методом – вытеснения воды или вытеснения воздуха – получают водород в этом приборе?
Почему невозможно получить и собрать водород, используя прибор, изображённый на другом рисунке?
Задание 8. Установите соответствие между названием химического вещества и областью его применения. К каждому элементу первого столбца подберите соответствующий элемент из второго столбца.
ВЕЩЕСТВО
А) серная кислота
Б) хлорид калия
В) алюминий
Г) водород
ПРИМЕНЕНИЕ
1) в авиации в составе лёгких сплавов
2) в автомобильных аккумуляторах
3) в качестве удобрения
4) средство для мытья посуды
5) топливо в ракетных двигателях
Задание 9. Из приведённого списка выберите верные суждения о правилах поведения в химической лаборатории и обращения с химическими веществами. В ответе запишите цифры, под которыми они указаны.
1) В химическом кабинете разрешается пробовать вещества на вкус.
2) Для получения разбавленных растворов серной кислоты концентрированную кислоту осторожно приливают к дистиллированной воде.
3) Если на лабораторном столе случайно загорелась тетрадка, то, чтобы потушить пламя, необходимо ограничить доступ воздуха к очагу возгорания, например накрыв тетрадь плотной тканью (полотенцем или тряпкой).
4) Если нет шпателя (ложечки), твёрдые реактивы можно брать руками.