Официальные задания и ответы школьного этапа 2023-2024 всероссийской олимпиады школьников Сириус по Химии 9 класс 04.10.2023
Задания и ответы ВсОШ Сириус по Химии 2023-2024 (04 октября 2023)
Приобрести задания и ответы (все варианты)
Задание 1:
В колбу Вюрца поместили кристаллы перманганата калия. Капельную воронку наполнили концентрированным раствором вещества А. Когда открыли кран капельной воронки, раствор А начал взаимодействовать с кристаллами перманганата калия в колбе Вюрца, при этом выделялся газ Б, простое вещество жёлто-зелёного цвета, и его собирали в цилиндр. Заполнив цилиндр на половину объёма, опыт прекратили.
В аппарат Киппа поместили гранулы цинка и залили раствор вещества А. При взаимодействии раствора А с цинком выделялся бесцветный газ В, который собирали в цилиндр, наполовину заполненный газом Б.
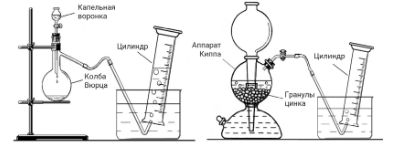
Цилиндр, заполненный смесью газов Б и В, неплотно закрыли пробкой, извлекли из ванны и осветили яркой вспышкой света. В результате очень быстрой реакции образовался газ A.
Газ А хорошо растворяется в воде. Раствор А реагирует с питьевой (пищевой) содой. В результате реакции выделяется газ Г, а в растворе образуется соль Д.
Запишите формулы веществ.
| А | |
| Б | |
| В | |
| Г | |
| Д |
Задание 2:
Вещество состоит из ионов, имеющих одинаковую электронную конфигурацию. Масса положительного иона более чем втрое превышает массу отрицательного иона.
Запишите формулу вещества.
Запишите электронную конфигурацию ионов, входящих в состав вещества (пример записи: 1s2 2s2 2p2). Строение каждого подуровня записывайте в отдельное поле, добавляя необходимое количество.
Задание 3:
Плотность водорода при опредёленных температуре и давлении равна 0.10 г/л. Смесь азота с неизвестным газом при этих же условиях имеет плотность 1.20 г/л. Какой это мог быть газ? Выберите все подходящие варианты:
Неон
Аргон
Аммиак
Углекислый газ
Задание 4:
Для лучевой терапии рака используют один из радиоактивных изотопов стронция. Его вводят в организм в виде растворимого хлорида, в котором массовая доля металла составляет 55.6%.
Определите массовое число изотопа.
Определите период его полураспада, если известно, что за 101 сутки распадается 75 % изотопа. Ответ выразите в сутках, округлите до десятых.
Задание 5:
Заполните пропуски химическими формулами.
При разложении соединения образовалось два простых вещества: 44.8 г металла и 47.04 л (н.у.) негорючего газа .
Задание 6:
Чтобы нагреть воздух в небольшой квартире на 1 градус Цельсия, требуется 200 кДж теплоты. Для этого можно использовать три вида топлива, теплоты сгорания которых приведены в таблице.
| Топливо | Водород H2 | Уголь C | Метан CH4 |
| Теплота сгорания, кДж/моль | 286 | 394 | 890 |
Какого топлива потребуется меньше всего по массе?
Угля
Водорода
Метана
Определите его массу. Ответ выразите в граммах, округлите до десятых.
Задание 7:
Оксид редкого металла, расположенного в третьей группе Периодической системы, имеет нежный розовый цвет. Массовая доля металла в оксиде равна 87.43 %.

Запишите порядковый номер неизвестного металла.
Запишите формулу оксида этого металла.
Задание 8:
Заполните пропуски химическими формулами и символами элементов.
Знаменитая скульптура Большого каскада Петергофа выполнена из сплава двух металлов __________ и ___________ , а снаружи покрыта золотом. Если образец такого сплава массой 10.0 г обработать соляной кислотой, то он растворится в ней лишь частично, выделив 1.2 л (н.у.) водорода и образовав 6.5 г твёрдого остатка —— розово-красного порошка _____________ , который темнеет на воздухе.
Если к образовавшемуся раствору по каплям добавлять раствор гидроксида натрия, наблюдается выпадение белого осадка вещества _____________, который растворяется в избытке щёлочи. Это вещество относится к классу ____________(Выбрать: оксидов/ оснований/ кислот/ амфотерных гидроксидов/ солей)
Ответ на задание 8
Задание 9:
Одной из первой химических реакций, осуществлённых человеком в древние времена, стал синтез синего пигмента, которого не существует в природе. Этот пигмент представляет собой кристаллическое вещество, состоящее из кальция, кремния, кислорода и неизвестного элемента X. Для получения пигмента использовали мел, малахит и кварцевый песок. Массовые доли элементов в синем пигменте: кальций —— 10.6 %; кремний —— 29.8 %; кислород —— 42.6 %.

Запишите химический символ элемента X.
Запишите химическую формулу синего пигмента, расположив элементы в порядке убывания их атомных масс.
Задание 10:
Лекарственный препарат, применяемый при расстройствах пищеварения, состоит из двух бинарных соединений магния: A и B. Массовая доля вещества A в этом препарате составляет 15 %, а B —— 85 %. При нагревании соединение A разлагается, превращаясь в B. Это превращение сопровождается выделением газа, простого вещества без цвета и без запаха. Тлеющая лучинка, внесённая в выделяющийся газ, ярко вспыхивает.
Если нагреть 28.0 г данного лекарственного препарата, то после полного превращения A в B масса твёрдого остатка составит 26.8 г.
Бинарные соединения —— вещества, состоящие из двух элементов.
Запишите формулы веществ A и B.
A:
B:
Какой объём газа (н.у.) выделяется при нагревании 28.0 г лекарственного препарата, описанного в условии задания? Ответ выразите в миллилитрах, округлите до целых.
Задание 11:
В пробирках, пронумерованных цифрами 1—5, выданы растворы следующих кислот: азотная, серная, хлороводородная, иодоводородная и сероводородная. Из каждой пробирки отобрали пробы растворов по 1 мл, к которым добавили бромную воду. В пробе из пробирки 1 наблюдалось появление интенсивной бурой окраски раствора. В пробе из пробирки 5 жёлто-бурая окраска бромной воды исчезла, раствор помутнел. В пробах из пробирок 2, 3 и 4 изменений не наблюдали.
Затем из пробирок 2, 3 и 4 снова отобрали пробы по 1 мл, к которым добавили раствор хлорида бария. Изменения наблюдались только в пробе из пробирки 3, в ней выпал осадок белого цвета. В пробирки 2 и 4 поместили по кусочку медной проволоки. В пробирке 2 изменений не наблюдалось, а в пробирке 4 медь начала растворяться, из раствора выделялся газ, буреющий на воздухе.
Установите соответствие между номерами и содержимым пробирок.
Иодоводородная кислота
Азотная кислота
Серная кислота
Хлороводородная кислота
Сероводородная кислота
Задание 12:
Частицы твёрдых веществ могут находиться во взвешенном состоянии в газообразной или жидкой среде, например, частички пыли в воздухе или частички глины в воде. При определённых условиях под действием силы тяжести частицы твёрдого вещества оседают, этот процесс называют седиментацией. Скорость оседания частиц, имеющих сферическую форму, описывается уравнением: v=29⋅r2(ρ−ρ0)gη,
где v —— скорость оседания частиц, r —— радиус частиц, ρ —— плотность частиц вещества, находящихся во взвешенном состоянии, ρ0 —— плотность среды, η —— вязкость среды, g —— ускорение свободного падения.
Исследовали оседание частичек пыли в воздухе. Какие частички пыли оседают быстрее?
Крупные
Мелкие
Одинаково
Недостаточно данных
Имеется смесь мелких частиц золота и речного песка, близких по размерам. Смесь высыпали в воду. Какие частицы оседают быстрее?
Частицы золота
Частицы речного песка
Одинаково
Недостаточно данных
Исследовали седиментацию частиц кварца в воде. Затем повторили опыт, предварительно растворив в воде сахар. Как изменилась скорость оседания частиц кварца?
Увеличилась
Уменьшилась
Не изменилась
Имеются две партии микроскопических частиц золота сферической формы. Радиусы частиц в первой партии в два раза больше, чем во второй. Золотые частицы из обеих партий поместили в воду. Что наблюдалось?
Частицы золота из разных партий оседают с одинаковой скоростью
Частицы из первой партии оседают в два раза быстрее
Частицы из первой партии оседают в четыре раза быстрее