
Олимпиада «Сириус» ответы, вопросы по Химии 9 класс, школьный этапа Всероссийской олимпиады 3 группа от 13 октября 2025 года. Официальный вариант с вопросами по химическим элементам, простым и сложным веществам.
Сириус по Химии для 3-ей группы 13 октября 2025 г.
Вопросы и ответы 9 класс
Задание 1. Неизвестный химический элемент X содержит на внешнем энергетическом уровне 2 электрона и имеет высшую степень окисления +7. Общее число протонов в ядре атома X не превышает 30.
Запишите химический символ элемента X.
Запишите химическую формулу высшего гидроксида элемента X.
При взаимодействии 11 г X с избытком соляной кислоты выделилось 4.48 л (н. у.) водорода. Запишите химическую формулу второго продукта реакции.
Найдите массу второго продукта реакции. Ответ выразите в граммах, округлите до десятых.
Правильный ответ: Mn, Mn(OH)7, MnCl2, 25.2
Задание 2. Имеются четыре твёрдых вещества: хлорид натрия, гидроксид натрия, сахар, нитрат кальция. Приготовили образцы этих веществ равной массы и растворили по отдельности в четырёх стаканах, содержащих равные объёмы воды. Расположите полученные растворы в порядке увеличения количества ионов в них.
Сахар
Хлорид натрия
Гидроксид натрия
Нитрат кальция
Правильный ответ: Сахар → Нитрат кальция → Хлорид натрия → Гидроксид натрия
Задание 3. Неизвестный газ X, поддерживающий горение, при пропускании над катализатором полностью разложился, образовав газовую смесь двух простых веществ, также поддерживающую горение. Объём смеси в 1.5 раза больше объёма X при одинаковых условиях. После пропускания смеси над раскалёнными медными стружками в газовой фазе осталось только вещество Y, которое в 7 раз тяжелее гелия. Объёмы газов X и Y одинаковы. Запишите формулы неизвестных веществ.
Формула вещества X:
Формула вещества Y:
Составьте уравнение разложения. В ответ запишите сумму наименьших целочисленных коэффициентов.
→ Раскрыть ответ
Задание 4. На школьной олимпиаде по химии 1940 года была предложена задача.
«Как из углемедной соли CuCO3⋅Cu(OH)2 получить медь? Напишите равенства реакций и нарисуйте схемы приборов (или одного прибора), необходимых для выполнения опыта.» Решение довольно простое: надо прокалить углемедную соль (современное название гидроксокарбонат меди) в токе газа.
Какие газы можно использовать для получения меди в данном опыте?
Запишите формулы двух газообразных (в условиях опыта) продуктов реакции.
Продукт 1:
Продукт 2:
→ Раскрыть ответ
Задание 5. В лабораторном опыте смешали равные объёмы растворов 0.05 М H2SO4, 0.01 М BaCl2 и 0.02 M K2CO3. Опишите результаты опыта:
Выпадают и BaSO4, и BaCO3
Выпадает BaCO3
Осадок не выпадает
Выпадает BaSO4 Масса полученного раствора масс исходных растворов.
Охарактеризуйте реакцию среды в образовавшемся растворе:
Кислая
Нейтральная
Щелочная
→ Раскрыть ответ
Задание 6. При обжиге 3.803.80 г смеси сульфидов марганца MnS и MnS2 образовались только сернистый газ объёмом 1.12л (н. у.) и твёрдый оксид марганца, содержащий 72 % металла по массе.
Запишите формулу оксида.
Определите массовую долю MnS в смеси. Ответ выразите в процентах, округлите до десятых.
→ Раскрыть ответ
Задание 7. Один из первых радионуклидов, используемых в радиомедицине в качестве источника гамма‑излучения уже более 80 лет, —131. Его получают бомбардировкой нейтронами некоторого нуклида AX с последующим β распадом (испусканием электрона) по схеме:
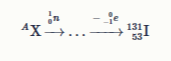
Запишите химический символ нуклида X.
Определите массовое число нуклида X.
→ Раскрыть ответ
Задание 8. Неизвестная кислота состоит из трёх элементов, степени окисления которых, взятые по модулю, образуют геометрическую прогрессию. В составе кислоты элементы, у которых электронами заняты не больше двух уровней.
Запишите формулу этой кислоты:
Определите степени окисления элементов в составе кислоты, располагая элементы в порядке возрастания атомной массы.
| Символ элемента: Степень окисления: |
Задание 9. Дан график зависимости плотности раствора от массовой доли этилового спирта и уксусной кислоты.
В три одинаковых стакана налили по 200 мл следующих жидкостей: вода, раствор этилового спирта и раствор уксусной кислоты. Стаканы с содержимым взвесили, результаты приведены в таблице. Зная массу стакана, определите его содержимое.
| Масса стакана, г | Содержимое стакана |
| 220.8 | |
| 237.0 | |
| 230.0 |
Определите массовые доли этилового спирта и уксусной кислоты в растворах. Ответы выразите в процентах, округлите до целых.
| Исследуемая жидкость | Массовая доля растворённого вещества, % |
| Раствор этилового спирта | |
| Раствор уксусной кислоты |
Задание 10. В пяти стаканах были выданы следующие вещества в виде тонко измельчённых порошков белого цвета: поваренная соль, кристаллическая сода (десятиводный кристаллогидрат карбоната натрия), мел, гипс (двуводный кристаллогидрат сульфата кальция) и сахар (сахароза). Результаты исследования выданных веществ представлены в таблице./Установите соответствие между номером стакана и его содержимым.
1
2
3
4
5
Поваренная соль
Кристаллическая сода
Мел
Гипс
Сахар
→ Раскрыть ответ
Список регионов, ответы к олимпиаде «Сириус» 3-ей группы
Данную работу пишут в следующих регионах: Астраханская область (30 регион), Курганская область (45 регион), Омская область (55 регион), Оренбургская область (56 регион), Пермский край (59 регион), Республика Башкортостан (02 регион), Самарская область (63 регион), Саратовская область (64 регион), Свердловская область (66 регион), Тюменская область (72 регион), Удмуртская Республика (18 регион), Ульяновская область (73 регион), Ханты-Мансийский автономный округ — Югра (86 регион), Челябинская область (74 регион), Ямало-Ненецкий автономный округ (89 регион)